大動脈ステントグラフト治療の現況
沖縄県立南部医療センター・こども医療センター血管内治療センター
我那覇 文清、久貝 忠男、摩文仁 克人、稲福 斉、末田 智紀
【要 旨】
大動脈瘤に対するステントグラフト治療は、従来の手術と比べ低侵襲で合併症も 少ない新しい治療法として世界的に脚光を浴び、急速に普及しつつある。現在わが 国で保険適応とされているものは胸部および腹部大動脈瘤であるが、今後適応は拡 大していくであろう。本稿では、前半で初学者向けにステントグラフト治療の方法 や特徴などの概要を述べた。後半では胸部および腹部大動脈瘤の治療成績を中心に、 またそれ以外にも治療対象と考えられる胸腹部大動脈瘤、大動脈解離、穿通性動脈 硬化性潰瘍、外傷などについてもより詳しく解説した。
はじめに
大動脈病変に対するステントグラフト(SG) 留置術は、鼠径部の小切開のみでアプローチで き開胸や開腹を要さず、また従来の手術と比べ 合併症も少ない画期的な治療法であり、企業製 造デバイスの市販に伴い世界中で急速に普及し つつある。米国での腹部大動脈瘤の治療 概況を例に挙げると、2000 年では人工血 管置換術による外科手術が治療件数の9 割を占めSG 治療は1 割に過ぎなかった が、わずか4 年後の2004 年には半数、 2006 年には約6 割がSG により治療され るようになった1)。わが国では1994 年頃 から一部の施設においてハンドメイドデ バイスを用いたSG 治療が開始され2)~ 5)、 2002 年には手技料の保険算定が認められ たが、欧米諸国に比べ市販デバイスの導 入が5 年以上も遅れたため施行可能な施 設は限られていた。しかし2007 年以降、 市販デバイスが利用できるようになった のを契機に裾野が一気に広がり、本格的 なSG 治療の時代が到来した。
(1)SG 治療の概要
【SG とは】
ステントグラフト(SG)とは金属製の自己 拡張型ステントを骨格としてその内側または外 側に人工血管を縫いつけたもので(図1)、血管 内で瘤をカバーするように留置し、血流を遮断することにより瘤の拡大・破裂を防ぐものであ る。大動脈病変に用いる市販のSG は6 ~ 8 ㎜ 径のデリバリーシステムに収納されており、通 常大腿動脈からガイドワイヤーを通して挿入 し、病変部へ運んで拡張させて留置する。
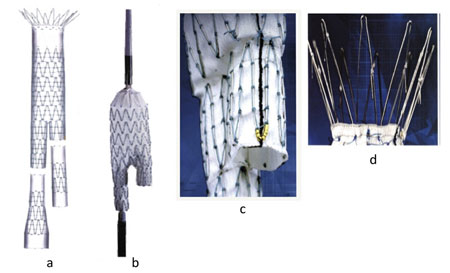
図1 ステントグラフト(例:腹部大動脈瘤治療用のCook 社製ゼニスAAA
エンドバスキュラーグラフト)
a :メインボディ(22 ~ 33mm 径)、同側および対側脚の3ピース構造。
b : 18Fr.または20Fr.のデリバリーシステムに収納されている。図はデリ
バリーシステムから展開したところ。
c :人工血管(ダクロン)の外側に金属ステント骨格が縫着されている。グラフト端にゴールドマーカーがあり、透視でよく視認できる。
d :ステントグラフトの頭側には、大動脈壁にくい込み位置ずれを防止する
フックのついた非被覆ステント部分がある。
【適応】
市販デバイスでは現在のところ使用対象を胸 部および腹部大動脈瘤に限定しており、原則と して治療適応はその両者となる。一方、SG 治 療を先進的に行ってきた施設においては様々な 大動脈疾患に対してSG 治療が試みられてお り、その詳細は後半で詳述したい。
【解剖学的適格条件】
SG 留置では胸部および腹部大動脈瘤患者の すべてが治療可能というわけではなく、一定の 解剖学的条件を満たす必要がある。たとえば瘤 近くに主要な分枝(弓部では左鎖骨下動脈、胸 部下行では腹腔動脈、腹部では腎動脈など)が 起始している場合は、SG のシーリングゾーンが 確保できずエンドリーク(注釈)の原因となる ために原則としては適応外となるし、大動脈の 屈曲が高度な場合はSG が追従せず留置不能と なる。またデバイスを挿入するアクセスは大腿 動脈が主となるが、アクセスから病変部までに 狭窄があったり高度の動脈硬化性変化がある場 合も不適切と判断される。市販デバイスにおい ては、SG をランディングさせる大動脈や腸骨動 脈の口径や長さ、瘤の屈曲角度など詳しい解剖 学的適応基準をそれぞれが設けており、その条 件の範囲内でないと原則的には使用できない。
-------------------------------------
(注釈:エンドリーク)
治療後グラフト周囲の瘤内に血流が残存する ことをエンドリークといい、SG 治療特有の治 療不成功因子である。SG と血管壁の接合部で の漏れ(type I)、腰動脈や下腸間膜動脈など SG で塞いだ分枝から瘤内への逆行性血流の残 存(type II)、SG 同志の接合部での漏れやグ ラフト破損による漏れ(type III)、グラフトの 多孔性による漏れ(type IV)の4 つに分類さ れる。これが生じると瘤内圧が低下せず破裂の可能性を残すことになるため遠隔期の成績に影 響し、場合によっては追加治療を要する。発生 率は対象者やデバイスにもよる6)が、治療後早 期のエンドリークは腹部、胸部大動脈瘤ともに 10 %前後である7)~ 13)。
-------------------------------------
【治療の実際】
術前計画:
マルチスライスCT 機による造影CT 検査を 行い、高精度の3D 画像やMPR 画像(任意の断 面の再構成画像)をワークステーション上で作 成する。まず瘤の形態や瘤壁性状(粥腫、壁在 血栓、石灰化の有無など)を把握し、次にデバ イスサイズを決めるのに必要な血管径や距離を 計測する。画像診断技術を駆使した術前の正確 なサイズ計測とそれに基づいたデバイス選択は、 本治療の成否を決める重要なポイントである。
麻酔法:
局所麻酔でも施行可能であるが、体動の制御 や呼吸止め、SG を大動脈内で展開する際の血 圧コントロールなどが容易な全身麻酔で行われ ることが多い。治療は手術室または血管造影室 で施行される。万一のopen surgery への移行 が容易で清潔面でも有利なのは手術室である が、本法は画像ガイド下に行われるため高精度 の画像機器を擁する血管造影室で行う施設も少 なくない。
留置手技:
腹部大動脈瘤と胸部大動脈瘤とでは留置方法 が異なりまたデバイスによって手順も違うが、 ここでは腹部大動脈瘤に対する2 ピース構造の SG 留置を例にとり手技を説明する(図2)。
- 1)両側鼠径部切開(5cm 程度)にて大腿動脈 を露出。
- 2)右大腿動脈を穿刺または切開し、ガイドワ イヤーを用いてSG メインボディが収納さ れたデリバリーシステム(6 ~ 7mm 径)を 瘤まで進める。
- 3) SG メインボディが瘤を完全に覆い、かつ腎 動脈を塞がない位置であることを造影で確 認。収納されたSG を開放し、腎動脈下大動脈から同側腸骨動脈に展開する(図2a)。
- 4) SG メインボディには対側脚を迎え入れるゲ ートが開いており、左大腿動脈からガイド ワイヤーをゲート内に挿入し対側脚のデリ バリーシステムを進め(図2b)、対側脚をゲ ート内から腸骨動脈まで展開する(図2c)。
- 5)これで逆Y 字型にSG が留置されたが、 SG と血管壁、SG 同士の接合部でバルー ン拡張を行い、SG を密着させエンドリー クを防止する。
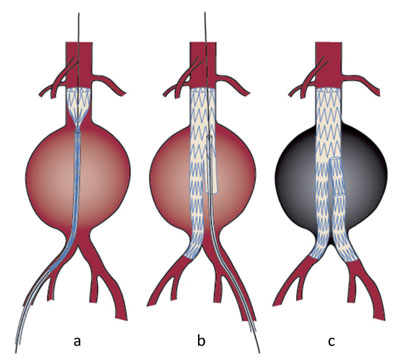
図2 腹部大動脈瘤に対するステントグラフト留置術
大動脈瘤・大動脈解離診療ガイドライン(2006 年改訂
版)より一部改変
a :右大腿動脈を切開し、ガイドワイヤーを用いてデリバリー
システムを進め、瘤内でステントグラフト拡張を開始する。
b :ステントグラフトメインボディを全展開したところ。メイ
ンボディには対側脚を迎え入れるゲートが開いており、左
大腿動脈からガイドワイヤーをゲート内に挿入し、対側脚
のデリバリーシステムを進める。
c :ゲート内から腸骨動脈まで対側脚を展開し、逆Y 字型にス
テントグラフトが留置された。
なお胸部大動脈では、SG 口径が腹部用より 大きくその分デリバリーシステムも太くなり、 また大腿腸骨動脈のアクセスから留置目的部位 までの距離の長いためデリバリーシステムをう まく進める工夫が必要で、ガイドワイヤーの pull through 法が用いられる。これは右上腕動 脈から腹部大動脈まで下ろしたガイドワイヤー を、大腿動脈側から入れたスネアカテーテルを 用いて捕獲し、大腿動脈から引き出して1 本の 長いガイドワイヤー(400cm)が上腕動脈~大 動脈~大腿動脈を通過する状態にするもので、 ガイドワイヤーのサポート性が格段に向上す る。このため効率よく押す力が伝わりデリバリ ーシステムをうまく進めることができ、また大 動脈弓部の彎曲にも大動脈軸に沿ってシステム を進められるためより安全である。
自験例:
自験例を供覧する。89 歳男性。高齢だが日 常生活における活動性は保たれていた。腹部大 動脈瘤は径5cm であった(図3a)。半年の経過 観察で増大傾向を示し要治療と判断されたが、 慢性肺気腫があり呼吸機能が悪くSG 治療を選 択した。静脈麻酔および局所麻酔下に両側鼠径 部を切開し、大腿動脈よりSG 留置術を行った (図3b)。手術時間は80 分で、出血量は200ml 以内であった。術後の回復は早く、翌日からは 食事を開始し、2 日後から歩行可能となった。 微熱と両側鼠径部の創痛はあったが自然軽快 し、6 日後には退院。退院後は速やかに元の生 活に復した。術後半年が経過したがエンドリー クもなく、経過観察中である。
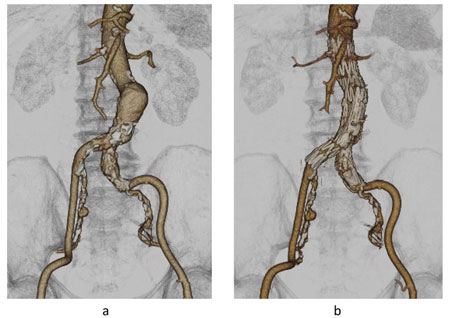
図3 自験例(ゼニスAAA エンドバスキュラーグラフト使用)
a :ステントグラフト術前の造影3 D-CT。腎動脈下に腹部大
動脈瘤を認める。
b :術後の造影3 D-CT 。大動脈から両側総腸骨動脈にかけて
逆Y 字型にステントグラフト留置が行われ、金属のステン
ト骨格が認められる。最頭側のステントは腎動脈にかかっ
ているが、この部分はグラフトに被覆されておらず、腎動
脈の血流は保たれている。
【治療後の瘤の変化】
治療後も瘤は切除されずに残存することが外 科手術と大きく異なる点である。瘤縮小の速度 は人工血管の厚さや透過性に影響を受けデバイ スによって多少違いがある14)が、腹部大動脈瘤 ではエンドリークがなくても1 年後に5mm 以上 の縮小を示すものは5 ~ 7 割程度で、3 ~ 4 割程度は瘤径の変化は認めない15)。その後も瘤の縮 小速度は通常緩徐であり、年単位で進行する。
【長所と短所】
これまで述べてきたSG 治療の特性と次項で 解説する事柄も含め、本治療の長所と短所を表 にまとめる(表1)。
表1 ステントグラフト治療の長所と短所

(2)対象疾患とその成績
前述のように市販デバイスが使用可能な大動 脈病変は胸部および腹部大動脈瘤のみであるが、 他にもSG 治療の有用性が認められているもの は少なくない。それらも含めて治療対象を列挙 し(表2)、以下それぞれについて概説する。
表2 大動脈ステントグラフト治療の対象疾患

【腹部大動脈瘤】
腹部大動脈瘤に対するSG 治療は、英国の EVAR trial16)やオランダのDREAM trial17)な どの大規模なランダム化比較試験により外科手 術に比べて周術期死亡や合併症が少ないことが 証明されており、SG 治療の安全性が高いエビ デンスレベルで示された分野といえる。最近の 米国での各群2 万人規模の比較研究18)(マッチ ングしたSG 治療群および外科手術群の比較) でも、周術期死亡率は外科手術群の4.8 %に対 してSG 群は1.2 %と有意に低く、周術期合併 症も心筋梗塞、肺炎、腎不全、腸管虚血、出 血、グラフト感染などいずれもSG 群で有意に 少なかった。一方、瘤を切除しないSG では長 期成績が問題になるが、遠隔期の瘤破裂は4 年 累計で外科手術群0.5 %に対してSG 群では 1.8 %と有意に高かった。しかし生存曲線を両 群で比較すると、SG 群の初期生存の優位性は3 年以上持続していた。とくに85 歳以上でその優 位性が顕著であり、高齢者でSG 治療の恩恵が 大きいことが示唆された。遠隔成績については 今後もあらゆる角度からの検討が必要であろう。
SG 治療後の回復の早さは特筆すべきものが ある。本邦での臨床試験7)をみると、術後経口 摂取開始までは0 . 9 ± 1 . 1 日、歩行開始は 1.8 ± 1.6 日であり数日以内に離床している。 われわれの経験でも術後人工物留置に伴う反応 熱や創痛はあるが、1 週間前後で退院可能なレ ベルに回復し、退院後も早期に元の生活に復し ている。特に高齢者の治療において、この回復 の早さは大きな利点と思われる。
治療対象者は、原則として外科手術のハイリ スク症例(虚血性心疾患、呼吸器障害、高齢、 開腹術の既往など)である。現在のところ切迫 破裂・破裂例は適応外とされている。瘤径とし ては、手術と同様に50mm 以上が絶対的適応で あるが、瘤の形態や増大スピード、破裂リスク 因子(高血圧、女性、喫煙、COLD など)の 有無も考慮されよう19)。
現在わが国で認可された腹部用の市販デバイ スはCook 社製ゼニス、Gore 社製エクスクルー ダー、Endologix 社製パワーリンクの三つがあ り、それぞれに解剖学的適格条件が定められて いる。共通項としては、腸骨大腿動脈がSG の デリバリーシステムを挿入するのに十分な径を 有し、強い屈曲がないことが条件となる。また 腎動脈起始部から瘤頭側端までを中枢ネックと称しSG の近位固定部となるが、この部分にデ バイスが隙間なく展開し瘤の血流を遮断できな いとエンドリークを生じるため、中枢ネックの 長さ・径・角度が規定範囲内にあることも重要 な条件である。通常中枢ネック長は15mm 以上 が適応とされる。なおデバイスにはそれぞれ長 所短所があるので、それらを考慮したデバイス 選択は治療成功の鍵である。
【胸部大動脈瘤】
胸部大動脈瘤では腹部大動脈瘤に比べ手術侵 襲がより大きく、鼠径部の小切開のみでアプロ ーチできるSG 治療の有用性はさらに高い。特 に下行大動脈瘤は、解剖学的に弓部と比べると より直線的で大きな分枝もなくSG 留置の条件 が良い。一方外科手術は左開胸を要し侵襲性が 高く、10 %程度に生じる対麻痺(大動脈遮断 や術中術後の低血圧などによって生じる脊髄虚 血)など重篤な合併症が多い。従って胸部下行 大動脈は、臨床的にSG 治療の有用性が最も高 い部位と思われる。実際、胸部下行大動脈瘤に 対する外科手術とSG 治療(Gore 社製TAG 使 用)の多施設前向き比較試験11)によると、周術 期死亡率は手術の11.7 %に対してSG 治療は 2.1 %、脊髄梗塞は14 %に対して3 %、呼吸器 合併症は20 %に対して4 %、腎不全は13 %に 対して1 %であり、SG 治療は有意差をもって 周術期死亡および合併症が少なかった。このこ とは他の企業製造デバイスによる比較試験12),13) やWalsh らによるメタ解析20)でも同様の結果 であり、胸部下行大動脈瘤に対するSG 治療は 手術に比べ明らかに安全である。一方、術後1 ないし2 年間でエンドリークやSG 位置ずれ・ 破損などSG 特有の理由により再治療を要する 例が2 ~ 10.5 %程に生じる11)~ 13),21)ことは手 術にはない治療不成功因子として挙げられる が、手術でも出血や吻合部瘤などで再手術を要 する例もあり13)、再治療率は同等であったとい う報告21)もある。生存率については、1 年瘤関 連死亡率は手術の11.6 ~ 11.8 %に対しSG で は3.1 ~ 5.8 %と低かった12),13)。より長期での 予後の検討は未だ限られるが、2 年全生存率は 手術の64 ~ 76 %に対してSG では54 ~ 78 % とほぼ同等であった11),21)。今後も長期成績はみ ていく必要はあるが、総じて胸部下行大動脈瘤 におけるSG 治療の有用性は高く、症例を選べ ば手術に置き換わる治療法になりうる。
上行大動脈瘤は解剖学的にSG 治療の対象と はなり難い。一方弓部瘤では弓部置換術が標準 治療であるが、耐術能の悪いあるいは高度の動 脈硬化を伴ったハイリスク例に対し、弓部分枝 へバイパスを行った後に弓部瘤自体はSG で閉 鎖するという外科手術と血管内治療を組み合わ せた治療(ハイブリッド法)22)が最近試みられ ている。体外循環や大動脈遮断を避けられハイ リスク例でも合併症や周術期死亡が少ないこと が報告されている23)。また弓部から下行大動脈 へおよぶ広範な大動脈瘤では、まず上行グラフ ト置換と弓部分枝へバイパスを行い、次に術野 から順行性に挿入したSG で瘤を閉鎖するとい うオープンSG 法23),24)が用いられる。瘤遠位 でのグラフト吻合が不要となるため胸骨正中切 開のみで一期的に手技が完遂し、治療の低侵襲 化に寄与している。オープンSG 法は真性動脈 瘤のみならず大動脈解離においても有効な術式 である。経験の多い施設からは、周術期死亡 3.2 %、脳梗塞5.6 %、脊髄虚血6.3 %という優 れた手術成績と長期予後が報告されている24)。
瘤径からみた適応は人工血管置換術に準じ、 真性胸部大動脈瘤では瘤径5 ないし6cm 以上、 あるいは急速に増大を示すもの(10mm/年以 上)が治療適応となる。ただし瘤による圧迫症 状(気管、食道など)を伴う場合は、SG では 症状の改善が得られるとは限らず適応から外れ る。嚢状瘤や仮性瘤は小さくても破裂の危険性 が高いため、サイズに関わらず治療を検討すべ きである。
現在市販されている胸部大動脈瘤用のデバイ スはGore 社製TAG とMedtronic 社製タレン トがあり、それぞれ胸部下行大動脈瘤が対象で ある。解剖学的適格条件としては、胸部大動脈 用SG のデリバリーシステムは腹部用より太い ため、腸骨大腿動脈のアクセスルートが十分な径を有し強い屈曲がないことはより厳密に評価 されるべきである。左鎖骨下動脈または腹腔動 脈と瘤との距離が20mm 以上あり、十分な中枢 および末梢のシーリングゾーンが得られること も条件である。
【胸腹部大動脈瘤】
胸腹部大動脈瘤の手術は、開胸開腹を要し手 術侵襲は極めて高い。2006 年の日本胸部外科 学会の統計では周術期死亡率は13 %と依然高 く、合併症も対麻痺、呼吸不全、腎不全など重 篤なものが多い25)。従ってこの領域でSG を用 いた低侵襲治療が可能であれば、臨床的価値は 非常に高いと考えられる。最近では大動脈また は腸骨動脈から腹部分枝へのバイパス手術を行 い胸腹部大動脈瘤にはSG を内挿するハイブリ ッド治療が試みられている。手術ハイリスク例 でも周術期死亡率3.2 %、合併症発生率9.6 % と比較的良好な成績を示す報告23)もあるが、 明らかな改善なしとする報告26)もあり、今後の さらなる検討が必要である。現状でハイブリッ ド治療が有効と考えられるのは、合併症などで 耐術能が悪い待機例や切迫破裂への緊急対応時 であろう。一方、内臓動脈への枝を追加できる 開窓あるいは枝付きSG の試み27)が始まってお り今後が注目されている。
【大動脈解離】
急性大動脈解離では、スタンフォードB 型で 真腔狭窄により腹部臓器や下肢の循環不全を伴 った場合にSG によるエントリー閉鎖が著効す ることがある28)。また切迫破裂例にSG が用い られることもある。しかし急性期の解離内膜は 非常に脆弱であり、エントリー部にSG を留置 した途端に新たな内膜損傷が生じ病態を悪くす る可能性もあり29)、現在コンセンサスは得られ ていない。
慢性例では解離内膜が硬化しているためSG 留置による内膜損傷のリスクは低く、偽腔の拡 張・瘤化を示す症例でSG によるエントリー閉 鎖が行われている30),31)。
【穿通性動脈硬化性潰瘍 (penetrating atherosclerotic ulcer: PAU)
PAU はアテローム性潰瘍が内膜を穿通して 仮性動脈瘤化し限局した大動脈解離のような画 像所見を呈するもので、高度の動脈硬化を背景 に生じる32)。切迫破裂例や降圧療法等保存的観 察で増大するものでは早期治療が必要である。 PAU は胸部下行大動脈に好発するが、前述の ようにこの部位は解剖学的にSG 留置に適して おり、高齢者や心・脳血管疾患合併など手術ハ イリスク例が多いことからも、PAU はSG 留 置のよい適応と考えられている。実際報告例で も周術期死亡や合併症発生は明らかに少なく 33)、遠隔成績の報告34)はまだ限られているが今 後第一選択となりうる。
【外傷性大動脈損傷】
大動脈損傷の多くは大動脈峡部に生じるが35)、 この部位へのSG 留置は左鎖骨下動脈を塞ぐか バイパスする選択肢が許容できればさほど困難 ではなく、病変部前後のシーリングゾーンとな る大動脈壁は普通健常であるためSG 留置に適 している。ただその主原因は交通外傷や転落で あり、比較的若年者に多いためSG の長期耐久 性の問題が残る。しかし外科手術と異なり開 胸・大動脈遮断・体外循環・片肺換気を要さな いため、周術期死亡・対麻痺・脳梗塞が有意に 少ないことがメタ解析で示されており36)、少な くとも短期的には明らかに優れた方法である。 とくに肺挫傷、頭部外傷、実質臓器損傷などの 合併例では、術中抗凝固療法も最小限で済ませ られるSG 治療の利点は大きい。破裂例での問 題は、患者の解剖学的条件に合ったデバイスが その場にあって緊急対応が可能か否かである。
【その他】
人工血管置換術後の吻合部仮性動脈瘤は再手 術自体が困難なことも多く、本法のよい適応で ある37)。感染性大動脈瘤は感染巣を除去するこ となく人工物を留置することに疑問はあるが、 有効例の報告も散見され38)、手術困難な症例で の破裂予防・出血制御目的での使用は可能と思 われる。その他、進行食道癌による大動脈への腫瘍浸潤などに対する出血制御目的でも本法は 有効である39)。
(3)将来展望
米国の市中病院では、本法普及の結果腹部大 動脈瘤の破裂症例が半減したというデータがあ る40)。わが国ではSG 導入が米国より7 年程遅 れたわけであるが、今後順調に普及すれば近々 同様の傾向をみる可能性は高い。
より将来への展望としては、デバイスの進化 により大動脈疾患に対するSG 治療の適応はさ らに拡大していくであろう。その中で今後の発 展のポイントの一つは、胸部大動脈瘤の約半数 を占める弓部瘤であろう。現状では弓部分枝へ のバイパス術を併用したSG 留置で対応してい るが、この領域により良いデバイスが登場すれ ば臨床的意義は大きい。弓部分枝への血流維持 が可能な開窓型で、個々の弓部の解剖に合わせ てデバイス全体をカーブさせたナユタというデ バイスがある41)。東京医大グループにより開発 され現在国内で臨床試験が進行中であるが大い に期待されるデバイスである。
もう一つのポイントは広範型大動脈瘤と思わ れ、米国で胸腹部大動脈瘤に試みられている開 窓または枝付きSG27)はひとつの方向性と思わ れる。手術が困難なこのような症例にこそSG 治療の真価が発揮されるのが期待される。
まとめ
大動脈瘤におけるSG 治療の現況を概説し た。今後デバイスの改良により適応はさらに拡 大していくであろう。
1)McPhee JT, Hill JS, Eslami M. The impact of gender
on presentation, therapy, and mortality of abdominal
aortic aneurysm in the United States, 2001-2004. J
Vasc Surg 2007; 45:891-9.
2)Kato M, Ohnishi K, Kaneko M, et al. New graftimplanting
method for thoracic aortic aneurysm of
dissection with a stented graft. Circulation 1996;94
(Suppl II):II188-93.
3)Ishimaru S, Kawaguchi S, Koizumi N, et al.
Preliminary report on prediction of spinal cord
ischemia in endovascular repair of thoracic aortic
aneurysm by retrievable stent graft. J Thorac
Cardiovasc Surg 1998;115:811-8.
4)Inoue K, Sato M, Iwase T, et al. Clinical endovascular
placement of branched graft for type B dissection. J
Thorac Cardiovasc Surg 1996;112:1111-3.
5)緑川博文、星野俊一、岩谷文夫ら 大動脈瘤に対する
ステントグラフト内挿術の成績 日血外会誌
1999;8:34-44.
6)Abbruzzese TA, Kwolek CJ, Brewster DC, et al.
Outcomes following endovascular abdominal aneurysm
repair (EVAR): An anatomic and device-specific
analysis. J Vasc Surg 2008;48:19-28.
7)吉川公彦、坂口昇二、東浦渉ら 腹部大動脈瘤に対す
るゼニスAAA エンドバスキュラーグラフトの臨床治
験成績 J Jpn Coll Angiol 2007;47:53-63.
8)Greenberg RK, Chuter TAM, Sternbergh III WC, et
al. Zenith AAA endovascular graft: Intermediate-term
results of the US multicenter trial. 2004 J Vasc Surg
39:1209-18.
9)Matsumura J, Brewster DC, Makaroun MS, et al. A
multicenter controlled clinical trial of open versus
endovascular treatment of abdominal aortic aneurysm.
2003 J Vasc Surg 37:262-71.
10)Wang GJ, Carpenter JP. The powerlink system for
endovascular abdominal aortic aneurysm repair: Sixyear
results. J Vasc Surg 2008;48:33-45.
11)Bavaria JE, Appoo JJ, Makaroun MS, et al.
Endovascular stent grafting versus open surgical
repair of descending thoracic aortic aneurysms in
low-risk patients: A multicenter comparative trial. J
Thorac Cardiovasc Surg 2007;133:369-77.
12)Fairman RM, Criado F, Farber M, et al. Pivotal
results of the Medtronic Vascular Talent Thoracic
Stent Graft System: The VALOR trial. J Vasc Surg
2008;48:546-54.
13)Matsumura JS, Cambria RP, Dake MD, et al.
International controlled clinical trial of thoracic
endovascular aneurysm repair with the Zenith TX2
endovascular graft: 1-year results. J Vasc Surg
2008;47:247-57.
14)Bertges D, Chow K, Wyers MC, et al. Abdominal
aortic aneurysm size regression after endovascular
repair is endograft dependent. J Vasc Surg 2003
37;716-23.
15)Haider S, Najjar SF, Cho JS, et al. Sac behavior
after aneurysm treatment with the Gore Excluder
low-permeability aortic endoprosthesis: 12-month
comparison to the original Excluder device. J Vasc
Surg 2006;44:694-700.
16)The EVAR trial participants. Comparison of
endovascular aneurysm repair with open repair in
patients with abdominal aortic aneurysm (EVAR
trial 1) , 30-day operative mortality results:
Randomized controlled trial. Lancet 2004: 364; 843-
48.
17)Prinssen M, Verhoeven ELG, Buth J, et al. A
randomized trial comparing conventional and
endovascular repair of abdominal aortic aneurysms. N
Engl J Med 2004: 351; 1607-1618.
18)Schermerhorn ML, O’Malley AJ, Jhaveri A, et al.
Endovascular vs. open repair of abdominal aortic
aneurysms in the Medicare population. N Engl J Med
2008: 358; 464-474.
19)大動脈瘤・大動脈解離診療ガイドライン(2006 年改
訂版) Circulation Journal 2006: 70; s1569-1646.
20)Walsh SR, Tang TY, Sadat U, et al. Endovascular
stenting versus open surgery for thoracic aortic
disease: Systemic review and meta-analysis of
perioperative results.
J Vasc Surg 2008;47:1094-8.
21)Stone DH, Brewster DC, Kwolek CJ, et al. Stentgraft
versus open-surgical repair of the thoracic
aorta: Mid-term results. J Vasc Surg 2006;44:1188-
97.
22)Criado FJ, Clark NS, Barnatan MF. Stent graft
repair in the aortic arch and descending thoracic
aorta: A 4-year experience. J Vasc Surg
2002;36:1121-8.
23)Zhou W, Reardon M, Peden EK, et al. Hybrid
approach to complex thoracic aortic aneurysms in
high-risk patients: Surgical challenges and clinical
outcomes. J Vasc Surg 2006;44:688-93.
24)Shimamura K, Kuratani T, Matsumiya G, et al. Longterm
results of the open stent-grafting technique for
extended aortic arch disease. J Thorac Cardiovasc
Surg 2008 135:1261-9.
25)Cambia RP, Clouse D, Davison JK, et al.
Thoracoabdominal aneurysm repair: Results with 337
operations performed over a 15-year interval. Ann
Surg 2002;236:471-479.
26)Chiesa R, Tshomba Y, Melissano G, et al. Hybrid
approach to thoracoabdominal aortic aneurysms in
patients with prior aortic surgery. J Vasc Surg
2007;45:1128-35.
27)Roselli EE, Greenberg RK, Pfaff K, et al.
Endovascular treatment of thoracoabdominal aortic
aneurysms. J Thorac Cardiovasc Surg 2007
133:1474-82.
28)Dake MD, Kato N, Mitchell RS, et al. Endovascular
stent-graft placement for the treatment of acute
aortic dissection. N Engl J Med 1999;340:1546-1552.
29)Hansen CJ, Bui H, Donayre CE, et al. Complication of
endovascular repair of high-risk and emergent
descending thoracic aortic aneurysms and dissections.
J Vasc Surg 2004;40:228-34.
30)Nienaber CA, Fattori R, Lund G, et al. Nonsurgical
reconstruction of thoracic aortic dissection by stentgraft
placement. N Engl J Med 1999;340:1539-1545.
31)Kato N, Hirano T, Shimono T, et al. Treatment of
chronic aortic dissection by transluminal endovascular
stent-graft placement: preliminary results. J Vasc
Intervent Radiol 2001;12:835-840.
32)Stanson AW, Kazmier FJ, Hollier LH, et al:
Penetrating atherosclerotic ulcers of the thoracic
aorta: natural history and clinicopathologic
correlations. Ann Vasc Surg 1986; 1: 15-23.
33)Schoder M, Grabenwoger M, Holzenbein T, et al.
Endovascular stent-graft repair of complicated
penetrating atherosclerotic ulcers of the descending
thoracic aorta. J Vasc Surg 2002;36:720-726.
34)Demers P, MillerDC, Mitchell RS, et al. Stent-graft
repair of penetrating atherosclerotic ulcers in the
descending thoracic aorta: mid-term results. Ann
Thorac Surg 2004;77:81-86.
35)Kato N, Dake MD, Miller DC, et al. Traumatic
thoracic aortic aneurysm: treatment with endovascular
stent-grafts. Radiology 1997;205:657-662.
36)Tang GL, Tehrani HY, Usman A, et al. Reduced
mortality, paraplegia and stroke with stent graft
repair of blunt aortic transections: A modern metaanalysis.
J Vasc Surg 2008;47:671-5.
37)Sachdev U, Baril DT, Morrissey NJ, et al.
Endovascular repair of para-anastomotic aortic
aneurysms. J Vasc Surg 2007;46:636-41.
38)Ting ACW, Cheng SWK, Ho P, et al. Endovascular
stent graft repair for infected thoracic aortic
pseudoaneurysms-a durable option? J Vasc Surg
2006;44:701-5.
39)Ikeda Y, Morita N, Kurihara H, et al. A primary
aortoesophageal fistula due to esophageal carcinoma
successfully treated with endoluminal aortic
stentgrafting. J Thorac Cardiovasc Surg.
2006;131:486-7.
40)McIff EB, Smilanich RP, McIff D. EVAR in
Community Hospitals. Endovasc Today 2006;5:52-60.
41)川口 聡、重松 宏 胸部大動脈瘤に対するステント
グラフト内挿術Jpn J Intervent Radiol 2007;22:431-
435.
Q U E S T I O N !
問題:大動脈ステントグラフト治療について、正しいものを選べ。
- 1)ステントグラフト留置術は開胸や開腹を要 さず、鼠径部の小切開から経大腿動脈的に血 管内でアプローチできる低侵襲治療である。
- 2)本邦における保険適応は、胸部大動脈瘤と 腹部大動脈瘤である。
- 3)対象者のすべてに治療が可能というわけで はなく、解剖学的条件を満たす必要がある。
- 4)ステントグラフト治療が臨床的にとくに有 用と考えられる病変は、胸部下行大動脈瘤で ある。
A(1,3,4), B(1,2), C(2,3)
D(4 のみ), E(1-4 のすべて)
CORRECT ANSWER! 7月号(vol.45)の正解
パーキンソン病治療の新しい展開
問題:パーキンソン病で黒質緻密部のドパミン 細胞内に蓄積するレビー小体を構成する タンパク質を以下より選択してください。
- 1)タウ蛋白
- 2)パーキン蛋白
- 3)αシヌクレイン
- 4)アミロイドβ蛋白
正解 3)